歐盟「藥品法規包裹法案」(Pharma Package)重點說明與簡析

歐盟「藥品法規包裹法案」(Pharma Package)重點說明與簡析
資訊工業策進會科技法律研究所
2025年09月10日
歐盟理事會(the Council of the European Union)於2025年6月4日就歐盟「藥品法規包裹法案」(Pharma Package)取得一致立場,且正與歐洲議會及歐盟執委會展開三方協商(trilogue),以共同研議最終立法版本[1]。法案預計於2026年初進行表決,若順利通過且加上過渡期,最快將於2028年正式施行,並可能重塑歐盟藥品市場之上市與投資規劃。
壹、背景摘要
有鑑於歐盟現行的藥品法規制度,自2004年修正後施行至今已逾20年,難以充分回應公共衛生需求、藥品可及性落差以及國際市場競爭等多重挑戰。因此,歐盟執委會(European Commission, EC)於2023年4月公布「藥品法規包裹法案」,旨在強化藥品供應鏈穩定性、提升藥品創新與競爭力,以建立更公平、具韌性與永續性的歐洲醫藥市場[2]。而2024年4月歐洲議會(European Parliament)[3]、2025年6月歐盟理事會亦分別提出不同版本,以促進歐洲整合為單一藥品市場。
本次改革對生技製藥產業影響深遠,為協助我國製藥產業在進入歐洲市場前先行掌握相關動向,以下將進行重點說明與分析。
貳、立法重點與比較
一、藥品監管保護期間之修正
在本次藥品法規包裹法案中,有關藥品監管保護期間之修正,為歐盟執委會、歐洲議會與歐盟理事會分歧最大,也是外界高度關注之核心重點。首先,現行歐盟新藥保護是由8年資料專屬保護期(Regulatory Data Protection, RDP)[4]與2年市場獨占期(Market Exclusivity, ME)所構成[5],若於資料專屬保護期間內取得新適應症可再延長1年市場獨占期,亦即保護期共為10~11年。
歐盟執委會則提議將資料專屬保護期縮短至6年,並搭配延長誘因機制,最多可再延長3年,條件包含:
1.滿足現有醫療需求可延長0.5年。
2.藥品在所有歐盟成員國上市可延長2年。
3.進行比較性臨床試驗可延長0.5年。
此外,不同於現行制度將新適應症延長1年納入市場獨占期,歐盟執委會則提議將此移至資料專屬保護期,因此合併原有2年市場獨占期後,保護期共為8~12年。
反之,歐洲議會則擬將資料專屬保護期調整為7.5年,並同樣設有延長誘因機制,但總延長上限至多1年,條件包含:
1.滿足現有醫療需求可延長1年。
2.進行比較性臨床試驗可延長0.5年。
3.在歐盟境內透過公私協力進行研發可延長0.5年。
若公司另取得比現有療法更有顯著臨床優勢之新適應症,則原有2年市場獨占期可再延長1年,合併計算後保護期共為9.5~11.5年。
而歐盟理事會則不同於歐盟執委會、歐洲議會,選擇將資料專屬保護期維持現行8年,但無法再延長。然而,市場獨占期則提議縮減為1年,但若符合特定條件則可再延長至2年,合併計算後保護期共為9~10年。條件包括:
1.滿足現有醫療需求。
2.產品含有新活性物質,並同時符合以下3項要件:
(1)上市許可申請具關聯性且有證據基礎的比較性臨床試驗結果作為支持。
(2)在一個以上的歐盟成員國內進行臨床試驗。
(3)申請人須證明已優先於歐盟申請上市許可,或於首次向歐盟以外地區提出申請後90日內完成歐盟上市申請。
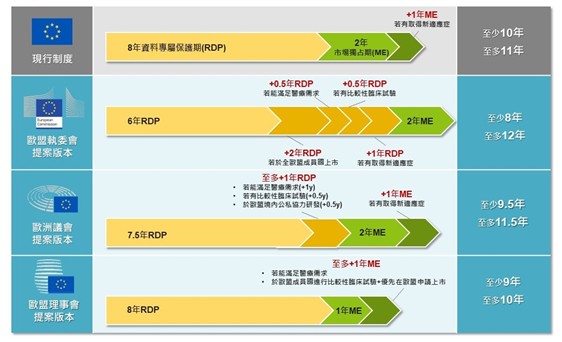
圖一、歐盟藥品法規包裹法案提議版本比較
資料來源:本研究整理
二、針對抗菌藥物引入創新研發機制
抗菌藥物抗藥性(Antimicrobial resistance, AMR)為近年全球公共衛生重要議題,並為世界衛生組織(World Health Organization, WHO)所列全球十大健康威脅之一[6]。因此,除嚴格限制抗菌藥物濫用外,為有效促進新型抗菌藥物之研發,本次藥品法規包裹法案中亦引入「可轉讓資料專屬保護權憑證」(Transferable Exclusivity Voucher, TEV)作為獎勵措施。
使用此憑證可賦予持有人額外1年資料專屬保護期,且除可用於抗菌藥品外,亦可適用於公司內其他更具商業價值藥品,或將此憑證轉賣給其他藥廠,為藥廠提供額外收入,但每張憑證僅能轉讓一次。
考量到憑證可能被用於商業利益龐大之藥品,藉此延緩學名藥與生物相似藥進入市場,並影響病患取得藥物之可及性,歐盟執委會於提議時亦強調此制度預計僅實施15年,或至多核發10張憑證後即停止適用[7]。此外,在歐盟執委會所提議之版本中,對於憑證使用亦設有限制,包含必須於憑證核發後5年內使用,且僅限用於尚在資料專屬保護期前4年之藥品,以確保市場可預測性。
歐洲議會與歐盟理事會雖然大致表態支持,但對憑證效力採取不同立場。歐洲議會態度較為保留,其提議使用憑證所額外延長之資料專屬保護期應依據抗菌藥品優先等級區分為6個月、9個月或12個月,且同樣受有總延長至多1年之限制。換言之,在歐洲議會提議版本下,無論延長事由為何,資料專屬保護期至多僅能延長至8.5年。
相對而言,歐盟理事會並未採納歐洲議會之提議,而是維持歐盟執委會提出增加1年資料專屬保護期之優惠設計。然而,為避免過度限制市場競爭,歐盟理事會亦新增規定,若憑證用於非抗菌藥品,則僅能在該藥品資料專屬保護期的第5年使用,且須證明過去4年內該藥品任一年銷售額均未超過4.9億歐元。
參、總結
「藥品法規包裹法案」反映出歐盟執委會、歐洲議會與歐盟理事會對新藥保護政策之差異,雖然三者皆試圖在鼓勵創新研發與提升藥品可近性之間取得平衡,但在藥品監管保護期間具體設計上仍有差異。歐盟執委會雖提議縮減資料專屬保護期,但也透過延長制度維持研發誘因。而歐洲議會則提議更高的初始保護門檻,但限制總延長期,且更著重在鼓勵研發活動而非市場擴張。至於歐盟理事會則維持現行保護年限,以持續激勵研發投入,但也透過縮短市場獨占期,加速學名藥與生物相似藥上市,以降低藥品價格並滿足醫療需求。
至於「可轉讓資料專屬保護權憑證」制度固然能為抗菌藥物提供研發誘因,但也伴隨著一定的潛在風險與利益分配爭議,如何確保該制度所帶來之公共利益超過公共衛生成本與風險,仍取決於未來最終立法版本應該如何調整與落實。對於我國製藥產業而言,此次改革有可能加速學名藥與生物相似藥進入歐洲市場,亦可能因延長誘因制度而遲延競爭時機,故仍應持續密切關注並審慎調整研發與市場策略。
[1]EUROPEAN COUNCIL, ‘Pharma package’: Council agrees its position on new rules for a fairer and more competitive EU pharmaceutical sector (2025), https://www.consilium.europa.eu/en/press/press-releases/2025/06/04/pharma-package-council-agrees-its-position-on-new-rules-for-a-fairer-and-more-competitive-eu-pharmaceutical-sector/#:~:text=The%20Council's%20position&text=obligation%20to%20supply%3A%20a%20new,patients%20in%20the%20member%20state (last visited Aug. 28, 2025).
[2]EUROPEAN COMMISSION [EC], Reform of the EU pharmaceutical legislation (2023), https://health.ec.europa.eu/medicinal-products/legal-framework-governing-medicinal-products-human-use-eu/reform-eu-pharmaceutical-legislation_en (last visited Aug. 28, 2025).
[3]EUROPEAN PARLIAMENT, Parliament adopts its position on EU pharmaceutical reform (2024), https://www.europarl.europa.eu/news/en/press-room/20240408IPR20308/parliament-adopts-its-position-on-eu-pharmaceutical-reform (last visited Aug. 28, 2025).
[4]「資料專屬保護期」是指專利藥提出新藥上市申請時,所檢附證明藥品安全性與療效之相關申請數據資料,其他藥廠非經原廠同意,於法定保護期間內不得引用,為行政機關針對原廠新藥上市申請資料給予之保護權益。詳請參考:台灣光鹽生物學苑,〈【醫藥小專欄】什麼是資料專屬權(data exclusivity)〉,台灣光鹽生物學苑,https://www.biotech-edu.com/%E3%80%90%E9%86%AB%E8%97%A5%E5%B0%8F%E5%B0%88%E6%AC%84%E3%80%91%E4%BB%80%E9%BA%BC%E6%98%AF%E8%B3%87%EF%A6%BE%E5%B0%88%E5%B1%AC%E6%AC%8A-data-exclusivity/ (最後瀏覽日:2025/08/28)。
[5]「市場獨占期」則是指在一定期間內,即使學名藥或生物相似藥已可向主管機關提出上市許可之申請並獲得核准,但仍不得實質上市銷售,須直到市場獨占期屆滿為止。市場獨占期與資料專屬保護期之比較,詳請參考:Specialist Pharmacy Service, Understanding data exclusivity and market protection (2025), https://www.sps.nhs.uk/articles/understanding-data-exclusivity-and-market-protection/ (last visited Aug. 28, 2025).
[6]〈世界抗生素週〉,衛生福利部疾病管制署,https://www.cdc.gov.tw/En/Category/MPage/t2VWXn93ooNVJPuQRF7jzg (最後瀏覽日:2025/08/28)
[7]CROWELL & MORING LLP, The New EU “Pharma Package”: The transferable exclusivity voucher—A comparison of Commission/Parliament/Council positions(2025),https://www.crowell.com/en/insights/client-alerts/the-new-eu-pharma-package-the-transferable-exclusivity-vouchera-comparison-of-commissionparliamentcouncil-positions (last visited Aug. 28, 2025).
歐盟執委會(European Commission)於2022年9月28日通過《人工智慧責任指令》(AI Liability Directive)之立法提案,以補充2021年4月通過之《人工智慧法》草案(Artificial Intelligence Act)。鑑於人工智慧產品之不透明性、複雜性且具自主行為等多項特徵,受損害者往往難以舉證並獲得因人工智慧所造成之損害賠償,《人工智慧責任指令》立法提案即為促使因人工智慧而受有損害者,得以更容易獲得賠償,並減輕受損害者請求損害賠償之舉證責任。 《人工智慧責任指令》透過引入兩個主要方式:(一)可推翻之推定(rebuttable presumptions):人工智慧責任指令透過「因果關係推定(presumption of causality)」來減輕受損害者之舉證責任(burden of proof)。受損害者(不論是個人、企業或組織)若能證明人工智慧系統因過失或不遵守法規要求之義務,致其受有損害(包括基本權利在內之生命、健康、財產或隱私等),並且該損害與人工智慧系統之表現具有因果關係,法院即可推定該過失或不遵守義務之行為造成受損害者之損害。相對的,人工智慧之供應商或開發商等也可提供相關證據證明其過失不可能造成損害,或該損害係由其他原因所致,以推翻該損害之推定。(二)證據揭露機制(disclosure of evidence mechanism):若受害者之損害涉及高風險人工智慧時,得要求自該供應商或開發商等處獲取證據之權利。受害者透過證據揭露機制能夠較容易地尋求法律賠償,並得以找出究責的對象。 歐盟執委會認為以安全為導向的《人工智慧法》,為人工智慧訂定橫向規則,旨在降低風險和防止損害,但仍需要《人工智慧責任指令》之責任規定,以確保損害風險出現時,相關賠償得以被實現。但歐盟執委會仍選擇了較小的干預手段,《人工智慧責任指令》針對過失之責任制度進行改革,並未採取舉證責任倒置(a reversal of the burden of proof)之作法,而是透過「可推翻之推定」,一方面減輕受損害者之舉證責任,使受損害者得對影響人工智慧系統並產生過失或侵害行為之人提出損害賠償;另一方面賦予人工智慧之供應商或開發商等有機會推翻前揭造成損害之推定,以避免人工智慧系統之供應商或開發商面臨更高的責任風險,可能阻礙人工智慧產品和服務創新。
新加坡擴大適用中小企業數位化政策以因應COVID-19疫情新加坡為實現「智慧國家」(Smart Nation)願景,長期致力於數位發展政策之推動。當中,在「協助產業加速數位化」方面,針對中小企業建置「中小企業數位化計畫」(SMEs Go Digital),並將其下「預先批准解決方案」(Pre-Approved Solutions)與「生產力解決方案補助金」(Productivity Solutions Grant, PSG)列為重要措施之一;甚而,於此波COVID-19疫情下,新加坡再度強化該等制度之運用,藉此加速中小企業數位發展進程。 所謂「預先批准解決方案」與「生產力解決方案補助金」,係指中小企業得透過企業科技庫(Tech Depot)網頁,了解中小企業數位化計畫下有哪些經過資通訊媒體發展管理局(Infocomm Media Development Authority, IMDA)預先批准的數位解決方案,並在取得供應商報價後,向新加坡企業發展局(Enterprise Singapore, ESG)申請「生產力解決方案補助金」之支援。於COVID-19疫情發生前,預先批准的數位解決方案包含「銷售與庫存管理」、「會計與文件管理」、「顧客關係管理」、「人力資源管理」、「網路安全」、「行動裝置門禁控制」及「車隊管理」等等13項系統,中小企業最高得享有報價70%的補助。 於COVID-19疫情發生後,除原有數位解決方案外,IMDA再預先批准下列內容,ESG亦於2020年4月1日到2020年12月31日間將所有方案的最高補助水平提升至80%,協助中小企業因應疫情並維持業務連續性: 遠距上班─線上協作工具(Online collaboration tools) 遠距上班─虛擬會議和電話工具(Virtual meeting and telephony tools) 訪客管理─佇列管理系統(Queue management system) 訪客管理─溫度檢測方案(Temperature screening solutions) 新加坡為因應COVID-19疫情,加強適用原有中小企業數位化計畫下的預先批准解決方案與生產力解決方案補助金,在既有制度上迅速地進行調整,以減緩疫情造成的產業衝擊,甚至加速中小企業數位發展之進程;另一方面,藉由COVID-19的特性,協助中小企業導入遠距上班與訪客管理等數位技術,改善過往因資金有限而未能優化營運基礎設備之難題,為中小企業開啟新的可能。
韓國《創業投資促進法》修正:明確創辦人連帶責任之適用範圍韓國國會於2025年11月21日通過《創業投資促進法》(Venture Investment Promotion Act, VIPA)修正,並於同年12月30日經總統公布,將過往僅屬行政指導層級,建議投資契約不宜要求創辦人對受投資企業依法應負擔的營運責任或債務義務負連帶保證責任,提升為具有法律拘束力之規範。 過去韓國雖透過行政指導方式,建議投資契約不宜要求創辦人負連帶保證責任,但因缺乏法律強制力,投資方常基於契約自由原則,仍在契約中要求創辦人擔保,造成風險不對等,影響創辦人創業意願。 修法後原則上不得將受投資企業依法應負擔的營運責任或債務義務強加於創辦人,透過法律規範,改善創辦人與投資方間的締約地位不對等,使投資風險更回歸企業本身之經營表現與事業前景之評估,進而提升新創團隊取得資本市場資源之效率。然而,為在制度保障與契約自由間取得平衡,若創辦人涉及提供虛假資訊、違反資金用途、違規處分股票或嚴重違約等故意或重大過失行為,該規範將不適用,投資方仍可請求創辦人履行連帶保證義務。 此外,本次修法後,創業育成機構、加速器、創投公司等與創辦人簽訂投資契約之情況下,不得要求創辦人就受投資企業依法應負擔之營運責任或債務義務負連帶保證責任,旨在於創投生態中建立統一風險分攤標準,釐清企業債務與個人財務界線。 本法預計於2026年7月1日生效,但有關明確創辦人連帶責任之適用範圍之條文,依附則規定自2025年12月30日公布日起即刻施行,從法律層面確立對創辦人的保護,改善韓國創投領域的責任歸屬制度。
美國產政研單位聯名向SEC請願,促請訂定企業應揭露其與氣候變遷有關的財務風險根據美國證券法規,上市公司、申請上市公司以及特定證券發行公司,應將其為符合美國聯邦、各州及地方環境法規所衍生,可能與公司之資本支出、營收與競爭地位有關之資料,向SEC提出並揭露予投資大眾;因為遵守相關環境法規而涉訟者,公司亦應揭露此等事實。除此之外,SEC規則亦要求,公司為符合環境法規所為之大規模資本支出,若可能對公司的清償能力產生重大影響,公司對於任何與之相關的已知發展趨勢、承諾的義務、事件或不確定性,亦應揭露之。 最近美國紐約州檢察長Andrew Cuomo向該州內五家能源公司發出傳票(subpoenas),要求這五家公司應各自分析其公司經營的氣候變遷風險,並將相關資訊揭露予投資大眾。此外,全美多個投資團體、十個州的財政官員以及環保團體亦聯名向美國證券交易委員會(Securities Exchange Commission, SEC)請願,促請SEC要求企業應該評估並揭露與氣候變遷有關的財務風險。請願者認為,氣候變遷相關資訊影響投資意願,亦為重要的公司資訊,故SEC應釐清,根據既有法規(即1934制定年的證券交易法)中的公司資訊揭露規定,公司亦應有揭露氣候變遷資訊之義務。 以上兩件事例的發展,隱含一個重要的跡象值得觀察,亦即未來美國SEC對於公司資訊揭露的管理,極可能涵蓋氣候變遷的風險資訊。雖然SEC目前尚未對請願事宜做出具體的表示,但有鑑於決策者已有越來越大的壓力必須正視全球氣候變遷問題,故SEC未來對於請願團體的回應及可能採取的措施,將代表公司應如何揭露氣候變遷風險資訊,始為適當。 此外,面對全球變遷所帶來的挑戰,美國許多州均積極提出或通過因應氣候變遷的法案,可預期企業經營者為遵循新一代的環境法規,未來將會有一波波的資金投入於法規遵循,目前企業經營者多將重心放在如何化挑戰為機會,然而公司在其中所為的投入,意味一定的財務風險,根據當前的發展,SEC極可能要求公司必須清楚地揭露此等氣候變遷相關資訊,值得企業經營者與投資人注意。雖然能源產業是氣候變遷風險最主要的揭露者,但氣候變遷風險實關乎所有的產業,目前已有許多保險公司也開始揭露其因為氣候變遷涉及的財務風險(如因颶風、水災、乾旱、火災或其他險惡的氣候現象所導致的財務損失)。



