歐盟「藥品法規包裹法案」(Pharma Package)重點說明與簡析

歐盟「藥品法規包裹法案」(Pharma Package)重點說明與簡析
資訊工業策進會科技法律研究所
2025年09月10日
歐盟理事會(the Council of the European Union)於2025年6月4日就歐盟「藥品法規包裹法案」(Pharma Package)取得一致立場,且正與歐洲議會及歐盟執委會展開三方協商(trilogue),以共同研議最終立法版本[1]。法案預計於2026年初進行表決,若順利通過且加上過渡期,最快將於2028年正式施行,並可能重塑歐盟藥品市場之上市與投資規劃。
壹、背景摘要
有鑑於歐盟現行的藥品法規制度,自2004年修正後施行至今已逾20年,難以充分回應公共衛生需求、藥品可及性落差以及國際市場競爭等多重挑戰。因此,歐盟執委會(European Commission, EC)於2023年4月公布「藥品法規包裹法案」,旨在強化藥品供應鏈穩定性、提升藥品創新與競爭力,以建立更公平、具韌性與永續性的歐洲醫藥市場[2]。而2024年4月歐洲議會(European Parliament)[3]、2025年6月歐盟理事會亦分別提出不同版本,以促進歐洲整合為單一藥品市場。
本次改革對生技製藥產業影響深遠,為協助我國製藥產業在進入歐洲市場前先行掌握相關動向,以下將進行重點說明與分析。
貳、立法重點與比較
一、藥品監管保護期間之修正
在本次藥品法規包裹法案中,有關藥品監管保護期間之修正,為歐盟執委會、歐洲議會與歐盟理事會分歧最大,也是外界高度關注之核心重點。首先,現行歐盟新藥保護是由8年資料專屬保護期(Regulatory Data Protection, RDP)[4]與2年市場獨占期(Market Exclusivity, ME)所構成[5],若於資料專屬保護期間內取得新適應症可再延長1年市場獨占期,亦即保護期共為10~11年。
歐盟執委會則提議將資料專屬保護期縮短至6年,並搭配延長誘因機制,最多可再延長3年,條件包含:
1.滿足現有醫療需求可延長0.5年。
2.藥品在所有歐盟成員國上市可延長2年。
3.進行比較性臨床試驗可延長0.5年。
此外,不同於現行制度將新適應症延長1年納入市場獨占期,歐盟執委會則提議將此移至資料專屬保護期,因此合併原有2年市場獨占期後,保護期共為8~12年。
反之,歐洲議會則擬將資料專屬保護期調整為7.5年,並同樣設有延長誘因機制,但總延長上限至多1年,條件包含:
1.滿足現有醫療需求可延長1年。
2.進行比較性臨床試驗可延長0.5年。
3.在歐盟境內透過公私協力進行研發可延長0.5年。
若公司另取得比現有療法更有顯著臨床優勢之新適應症,則原有2年市場獨占期可再延長1年,合併計算後保護期共為9.5~11.5年。
而歐盟理事會則不同於歐盟執委會、歐洲議會,選擇將資料專屬保護期維持現行8年,但無法再延長。然而,市場獨占期則提議縮減為1年,但若符合特定條件則可再延長至2年,合併計算後保護期共為9~10年。條件包括:
1.滿足現有醫療需求。
2.產品含有新活性物質,並同時符合以下3項要件:
(1)上市許可申請具關聯性且有證據基礎的比較性臨床試驗結果作為支持。
(2)在一個以上的歐盟成員國內進行臨床試驗。
(3)申請人須證明已優先於歐盟申請上市許可,或於首次向歐盟以外地區提出申請後90日內完成歐盟上市申請。
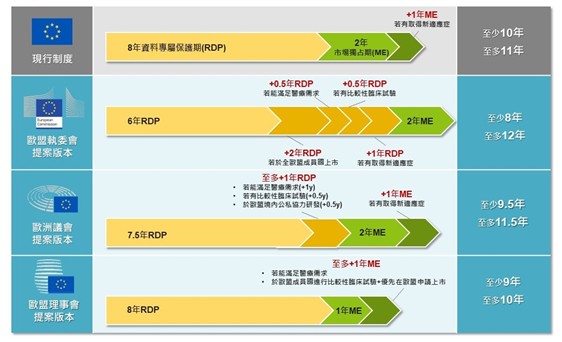
圖一、歐盟藥品法規包裹法案提議版本比較
資料來源:本研究整理
二、針對抗菌藥物引入創新研發機制
抗菌藥物抗藥性(Antimicrobial resistance, AMR)為近年全球公共衛生重要議題,並為世界衛生組織(World Health Organization, WHO)所列全球十大健康威脅之一[6]。因此,除嚴格限制抗菌藥物濫用外,為有效促進新型抗菌藥物之研發,本次藥品法規包裹法案中亦引入「可轉讓資料專屬保護權憑證」(Transferable Exclusivity Voucher, TEV)作為獎勵措施。
使用此憑證可賦予持有人額外1年資料專屬保護期,且除可用於抗菌藥品外,亦可適用於公司內其他更具商業價值藥品,或將此憑證轉賣給其他藥廠,為藥廠提供額外收入,但每張憑證僅能轉讓一次。
考量到憑證可能被用於商業利益龐大之藥品,藉此延緩學名藥與生物相似藥進入市場,並影響病患取得藥物之可及性,歐盟執委會於提議時亦強調此制度預計僅實施15年,或至多核發10張憑證後即停止適用[7]。此外,在歐盟執委會所提議之版本中,對於憑證使用亦設有限制,包含必須於憑證核發後5年內使用,且僅限用於尚在資料專屬保護期前4年之藥品,以確保市場可預測性。
歐洲議會與歐盟理事會雖然大致表態支持,但對憑證效力採取不同立場。歐洲議會態度較為保留,其提議使用憑證所額外延長之資料專屬保護期應依據抗菌藥品優先等級區分為6個月、9個月或12個月,且同樣受有總延長至多1年之限制。換言之,在歐洲議會提議版本下,無論延長事由為何,資料專屬保護期至多僅能延長至8.5年。
相對而言,歐盟理事會並未採納歐洲議會之提議,而是維持歐盟執委會提出增加1年資料專屬保護期之優惠設計。然而,為避免過度限制市場競爭,歐盟理事會亦新增規定,若憑證用於非抗菌藥品,則僅能在該藥品資料專屬保護期的第5年使用,且須證明過去4年內該藥品任一年銷售額均未超過4.9億歐元。
參、總結
「藥品法規包裹法案」反映出歐盟執委會、歐洲議會與歐盟理事會對新藥保護政策之差異,雖然三者皆試圖在鼓勵創新研發與提升藥品可近性之間取得平衡,但在藥品監管保護期間具體設計上仍有差異。歐盟執委會雖提議縮減資料專屬保護期,但也透過延長制度維持研發誘因。而歐洲議會則提議更高的初始保護門檻,但限制總延長期,且更著重在鼓勵研發活動而非市場擴張。至於歐盟理事會則維持現行保護年限,以持續激勵研發投入,但也透過縮短市場獨占期,加速學名藥與生物相似藥上市,以降低藥品價格並滿足醫療需求。
至於「可轉讓資料專屬保護權憑證」制度固然能為抗菌藥物提供研發誘因,但也伴隨著一定的潛在風險與利益分配爭議,如何確保該制度所帶來之公共利益超過公共衛生成本與風險,仍取決於未來最終立法版本應該如何調整與落實。對於我國製藥產業而言,此次改革有可能加速學名藥與生物相似藥進入歐洲市場,亦可能因延長誘因制度而遲延競爭時機,故仍應持續密切關注並審慎調整研發與市場策略。
[1]EUROPEAN COUNCIL, ‘Pharma package’: Council agrees its position on new rules for a fairer and more competitive EU pharmaceutical sector (2025), https://www.consilium.europa.eu/en/press/press-releases/2025/06/04/pharma-package-council-agrees-its-position-on-new-rules-for-a-fairer-and-more-competitive-eu-pharmaceutical-sector/#:~:text=The%20Council's%20position&text=obligation%20to%20supply%3A%20a%20new,patients%20in%20the%20member%20state (last visited Aug. 28, 2025).
[2]EUROPEAN COMMISSION [EC], Reform of the EU pharmaceutical legislation (2023), https://health.ec.europa.eu/medicinal-products/legal-framework-governing-medicinal-products-human-use-eu/reform-eu-pharmaceutical-legislation_en (last visited Aug. 28, 2025).
[3]EUROPEAN PARLIAMENT, Parliament adopts its position on EU pharmaceutical reform (2024), https://www.europarl.europa.eu/news/en/press-room/20240408IPR20308/parliament-adopts-its-position-on-eu-pharmaceutical-reform (last visited Aug. 28, 2025).
[4]「資料專屬保護期」是指專利藥提出新藥上市申請時,所檢附證明藥品安全性與療效之相關申請數據資料,其他藥廠非經原廠同意,於法定保護期間內不得引用,為行政機關針對原廠新藥上市申請資料給予之保護權益。詳請參考:台灣光鹽生物學苑,〈【醫藥小專欄】什麼是資料專屬權(data exclusivity)〉,台灣光鹽生物學苑,https://www.biotech-edu.com/%E3%80%90%E9%86%AB%E8%97%A5%E5%B0%8F%E5%B0%88%E6%AC%84%E3%80%91%E4%BB%80%E9%BA%BC%E6%98%AF%E8%B3%87%EF%A6%BE%E5%B0%88%E5%B1%AC%E6%AC%8A-data-exclusivity/ (最後瀏覽日:2025/08/28)。
[5]「市場獨占期」則是指在一定期間內,即使學名藥或生物相似藥已可向主管機關提出上市許可之申請並獲得核准,但仍不得實質上市銷售,須直到市場獨占期屆滿為止。市場獨占期與資料專屬保護期之比較,詳請參考:Specialist Pharmacy Service, Understanding data exclusivity and market protection (2025), https://www.sps.nhs.uk/articles/understanding-data-exclusivity-and-market-protection/ (last visited Aug. 28, 2025).
[6]〈世界抗生素週〉,衛生福利部疾病管制署,https://www.cdc.gov.tw/En/Category/MPage/t2VWXn93ooNVJPuQRF7jzg (最後瀏覽日:2025/08/28)
[7]CROWELL & MORING LLP, The New EU “Pharma Package”: The transferable exclusivity voucher—A comparison of Commission/Parliament/Council positions(2025),https://www.crowell.com/en/insights/client-alerts/the-new-eu-pharma-package-the-transferable-exclusivity-vouchera-comparison-of-commissionparliamentcouncil-positions (last visited Aug. 28, 2025).
歐洲理事會修訂「保護個人有關個人資料處理及自由流通規則(一般資料保護規則)」(Proposal for a Regulation of the European Parliament and of the Council on the protection of individuals with regard to the processing of personal data and on the free movement of such data (General Data Protection Regulation), GDPR),該草案內容包括行政罰鍰三審制(three-tiered system)。凡故意或過失違反歐洲資料保護基本權之企業,情節重大者,可能招致鉅額行政罰鍰,草案之裁罰性措施將讓從業者更加重視資料保護法益。 是否對違反GDPR之侵權行為裁處罰鍰,會員國政府有裁量權限;已受刑事制裁者,政府亦得免除罰鍰以避免重複處罰。資料保護主管機關(data protection authorities, DPAs)依三審制判斷,確保所裁處罰鍰具有效性、比例性及嚇阻性。三審制包括:第一審,是否對資料當事人之資料要求延遲、變更回應;第二審,是否對資料當事人、DPAs盡資訊透明義務;第三審,各種具體侵權行為,包括對於資料取得缺乏法律依據、未能即時告知資料違反情事,或未採取適當安全防衛措施於歐盟以外區域傳遞資料等。 依草案,DPAs審酌罰鍰額度時,應依下列計算罰鍰: (1) 企業故意或過失未能於一定期間內,回應資料當事人之資料查閱請求者,裁處上一會計年度全球總年營業額0.5%罰鍰。 (2) 企業故意或過失未能提供任何或所有符合資料當事人要求之必要資訊;或未能對消費者充分揭露個人資料蒐集、處理的目的者,裁處上一會計年度全球總年營業額1%罰鍰。 (3) 企業故意或過失未能維護消費者權益,更正或刪除消費者資料,違反GDPR所保障之消費者「被遺忘權」者,裁處上一會計年度全球總年營業額1%罰鍰。 (4) 企業故意或過失處理個人資料,行為不具適法性、違反法規、沒有對當事人通知資料違反或將個人資料傳遞自歐盟以外區域,該區域沒有適當安全資料保護者,就企業上一會計年度全球總年營業額裁處2%罰鍰。 六月中旬,歐盟各部長將就歐洲議會、歐盟理事會的提案,就罰鍰額度進行最後協商,未來將持續關注草案協商後續發展。
美國知名嘻哈歌手Dr. Dre對婦產科醫生的商標註冊提出異議遭駁回2015年美國賓州的一位婦產科醫生Draion M Burch(以下簡稱Burch)申請註冊「Dr. Drai」商標在國際商品服務類別41(教育及娛樂服務)及44(醫療諮詢服務)以行銷自身的有聲書籍及研討課程。美國知名的嘻哈歌手Dr. Dre認為,該商標與自身的「Dr. Dre」【已註冊國際商品服務類別9(系列音樂錄製)、16(海報、美術印刷及貼紙)、25(T恤、長袖衫、帽子)、41(由音樂藝術家及創作者提供之娛樂服務)】雖拼法不同但讀音相同,會引起消費者的混淆,因而向商標審理暨訴願委員會(Trademark Trail and Appeal Board, TTAB,下稱委員會)提出異議。 委員會認為,雖然「Dr. Dre」與「Dr. Drai」兩者類似,然而Dr. Dre無法證明消費者會因而被混淆、誤導,進而去購買Dr. Drai的商品。該意見書更指出,由於Burch醫生的演講費用是5000元美金,比起購買一般物品,消費者在購買Burch醫生的書籍或演講門票時會付出「較高的注意程度」。Burch醫生也辯稱,消費者不太可能會混淆這兩個商標,因為「Dr. Dre並非醫生,也沒有資格提供任何醫療服務或銷售醫藥、保健產品。」他更證稱從未想要利用Dr. Dre的名聲謀取利益,因Dr. Dre創作的歌詞顯示出其對某些族群的歧視,若消費者將他與Dr. Dre聯想,只會認為他是一位不好的醫生。 基於上述理由,委員會最後駁回歌手Dr. Dre的異議。Dr. Dre的律師James Weinberger目前對此案拒絕做出評論,也不願透漏是否會再提出上訴。 「本文同步刊登於TIPS網站(https://www.tips.org.tw)」
歐盟議會通過電信改革法案歐盟議會在2009年11月24日通過歐盟電信改革法案,其中包含12項重要改革: 1. 消費者要求以攜帶電話號碼方式變換電信公司時,只需一個工作日; 2. 強化對消費者資訊之傳達,包含使消費者充分知悉所訂購之服務內容、服務品質、賠償和退費機制; 3. 保障歐洲人民網路接取自由(Internet access); 4. 新的網路開放及網路中立(open and neutral net)保護措施,賦予國家及權責機關,得對網路服務之最低品質限度做出規範,且須於簽約前對消費者告知流量控管之技術,和該技術對其服務之影響; 5. 消費者個人資料保護及垃圾郵件(spam)之處理; 6. 更方便的緊急通訊服務; 7. 國家電信規範將更加獨立; 8. 新的歐洲電信主管機關將會協力確保公平競爭和電信市場規範之一致性; 9. 歐洲執委會被授予法規範補償制度之檢視權利; 10. 在面臨競爭問題時,國家通信機構可採取功能性分離(Function Separation)措施; 11. 加速全歐洲之寬頻接取普及率; 12. 鼓勵對下世代網路(NGA)之競爭與投資。 至於先前飽受爭議之三振法案,在多方溝通下,歐盟議會決議,人民之網路自由,是歐洲公民重要之權利,但在保護智慧財產權和藝術創作方面,需要找尋更新、更現代化,且更有效率的保護方法。至於切斷網際網路之服務,除非有「先前的、公正、無偏見」且「有效率並即時」的司法審訊程序,否則不應限制人民網路接取之權利。
個人資料受害該向誰求償?


